
Как мы уже давно знаем, природа является отличным источником вдохновения для многих исследований, открытий и экспериментов. Птицы и крылатые насекомые показали нам, что небо вполне достижимо, водные млекопитающие подсказали, как нам продлить свое пребывание под водой, а пауки доказали, что даже самые маленькие существа способны создавать нечто невероятное. В рассматриваемом нами сегодня исследовании ученые из института физико-химических исследований (Вако, Япония) нашли способ создавать искусственную паутину за счет фототрофных бактерий. Как именно они этого достигли, насколько натуральна полученная паутин и почему использовались именно фототрофные бактерии? Ответы на эти и другие вопросы ждут нас в докладе ученых. Поехали.
Основа исследования
Для многих людей пауки это «о Боже, уберите его с меня!» или «фу, какая гадость». Однако, отбросив фобии и предвзятое отношение к этим созданиям, можно рассмотреть, насколько уникальны эти восьминогие хищники. Анатомия пауков буквально создана для идеальной охоты. С одной стороны, есть яд, способный парализовать или даже убить добычу или неприятеля. С другой — отлично развитые органы чувств (особенно осязания за счет трихоботрий (волосков) по всему телу). Визитной карточкой пауков, ставшей основой для многих метафор и крылатых выражений, является их паутина.
Ролик о том, как пауки производят свою знаменитую паутину.
По своей сути, паутина это белок, состав которого богат на глицин (C2H5NO2), аланин (NH2-СH(СН3)-СООН) и серин (HO2C-CH(NH2)CH2OH). Образуется паутина в специальной железе, где пребывает в жидком виде.
Когда секрет железы выделяется наружу через многочисленные прядильные трубочки, специальные паутинные бородавки формируют из него нити, которые паук использует в строительстве своих смертоносных ловушек.
Нити паутины уникальны, ибо их механические характеристики превосходят многие другие материалы. К примеру, предел прочности на разрыв паутины у обыкновенного крестовика (Araneus diadematus) составляет 1.1-2.7 ГПа, у человеческого волоса — 0.25 ГПа, а у стали 0.4-1.5 ГПа. Плотность паучьего шелка составляет 1/6 плотности стали (1.3 г/см3). То есть, если обогнуть Землю паутиной, то ее вес составит всего лишь 500 грамм. Плотность энергии составляет примерно 1.2×108 Дж/м3. Также шелк пауков крайне пластичный, т.е. может растягиваться в 5 раз от изначальной длины (в расслабленном состоянии) без каких-либо разрывов. Ударная вязкость паутины сравнима с полиарамидными нитями. Пауки не относятся к экстремофилам, но их паутина может легко пережить температуру от -40 °C до 220 °C. Кроме того, биоразлагаемые и биосовместимые свойства шелка делают его пригодным для применения в медицинских целях.
Сравнение прочности на растяжение стальной нити и паучьего шелка (соответствующей плотности).
Любопытно и то, что один вид пауков может производить несколько разных по свойствам и применению типов паутины (пауки вида Argiope argentata производят целых 5 вариантов паутины):
- для внешних граней и каркаса паутины (очень прочная);
- для областей захвата добычи (очень липкая, эластичная и прочная);
- для кокона с потомством (напоминает затвердевший шелк);
- для обволакивания добычи (может быть в 2 или 3 раза прочнее каркасной паутины);
- для временных линий во время строительства основной паутины;
- для создания креплений между линиями паутины или между паутиной и местом ее крепления.
Это лишь краткое описание паучьего шелка, но и того достаточно, чтобы понять уникальность этого вещества. Именно потому многие ученые уже достаточно давно пытаются создать искусственный эквивалент паутины. У многих это вполне успешно получается. Однако остается нерешенной проблема массовости производства.
В рассматриваемом нами сегодня труде ученые предложили решение этой проблемы. Заключается оно в использовании пурпурной бактерии Rhodovulum sulfidophilum, обладающей свойствами как фототрофов*, так и галофилов*.
Фототрофы* — организмы, использующие свет для получения энергии.
Галофилы* — тип экстремофилов, обитающих в условиях высокой солености.R.sulfidophilum это морская аноксигенно фотосинтезирующая* бактерия с разными метаболическими особенностями, которая продуцирует биоводород, биопластик и внеклеточные нуклеиновые кислоты.
Аноксигенный фотосинтез* — в отличие от обычного фотосинтеза, в процессе аноксигенного не происходит образования молекулярного кислорода.Но самым важным для ученых навыком R.sulfidophilum является ее возможность расти в фотоавтотрофных условиях за счет использования недорогих и возобновляемых ресурсов, таких как свет (энергия), CO2 (источник углерода) и N2 (источник азота), посредством процессов фотосинтеза и фиксации азота. Кроме того R.sulfidophilum прекрасно чувствует себя в морской воде, что способствует снижению риска биологического загрязнения во время культивирования.
За последние годы был достигнут неплохой результат в массовом производстве спидроина (MaSp, белок паучьего шелка) с применением рекомбинантных организмов-хозяев (бактерия Escherichia coli, дрожжи Pichia pastoris, шелкопряд Bombyx mori, табак, культуры клеток млекопитающих и т.д.).
Авторы сего труда не отрицают успех своих предшественников, но отмечают крайне малые объемы производства и достаточно высокую стоимость конечного продукта из-за высокой стоимости самого производства (в случае микробной ферментации 70% затрат производства составляет сырье).
В своем исследовании авторы предлагают новую методику экономичного и эффективного производства паучьего шелка за счет бактерии R.sulfidophilum, способную продуцировать гидрофобную повторяющуюся последовательность MaSp1 (спидроин-1) с использованием небольшого количества органического вещества в условиях фотогетеротрофного или фотоавтотрофного роста.
Результаты исследования
Для начала необходимо было подготовить бактерии R.sulfidophilum.
Ранее сообщалось о возможности введения экзогенной плазмидной ДНК в R.sulfidophilum посредством бактериальной конъюгации* с использованием плазмид, полученных из pCF1010, и E.coli S17-1 в качестве донорного штамма.
Конъюгация* — однонаправленный перенос части генетического материала при непосредственном контакте двух бактериальных клеток.В данном исследовании было решено использовать другой вектор (pBBR1MCS-2), содержащий ген устойчивости к канамицину, ген mob, кодирующий специфическую нуклеазу, и источник переноса (oriT*), которые широко использовались в грамотрицательной бактериальной конъюгации.
oriT* представляет собой короткую последовательность (до 500 п.н.), необходимую для переноса содержащей ее ДНК от бактериального хозяина реципиенту во время бактериальной конъюгации.В хромосоме R.sulfidophilum (инвентарный номер NZ_CP015418) два гена устойчивости к теллуриту, кодирующие белок устойчивости к теллуриту семейства TerB, присутствовали в локусах «A6W98_RS06280» и «A6W98_RS17070».
Признаки устойчивости к канамицину и к теллуриту использовались в качестве маркеров для отбора положительных конъюгантов R.sulfidophilum.
Плазмида* pBBR1-Ptrc-MaSp1 содержала:
- промотор* trc (Ptrc), который является сильным гибридным конститутивным промотором в E.coli;
- последовательность «AGGAGA» области связывания рибосом (RBS);
- повторяющаяся последовательность доменов гена MaSp1 из Nephila clavipes, оптимизированная по кодонам (единица генетического кода) для E.coli (1a, 1b).
Плазмида* — небольшая молекула ДНК, отделенная от хромосом и способная к самостоятельной репликации.
Промотор* — последовательность нуклеотидов ДНК, опознаваемая РНК-полимеразой как место для начала транскрипции (синтез РНК из ДНК).Приблизительно 0.4 г влажной клеточной массы (CWM от cell wet mass) было получено из 50 мл рекомбинантной культуры R.sulfidophilum, выращенной до стационарной фазы роста в фотогетеротрофных условиях, а именно из морского бульона (MB от marine broth) со светодиодной подсветкой при (730 нм, 20–30 Вт/м2) в течение 4 дней.
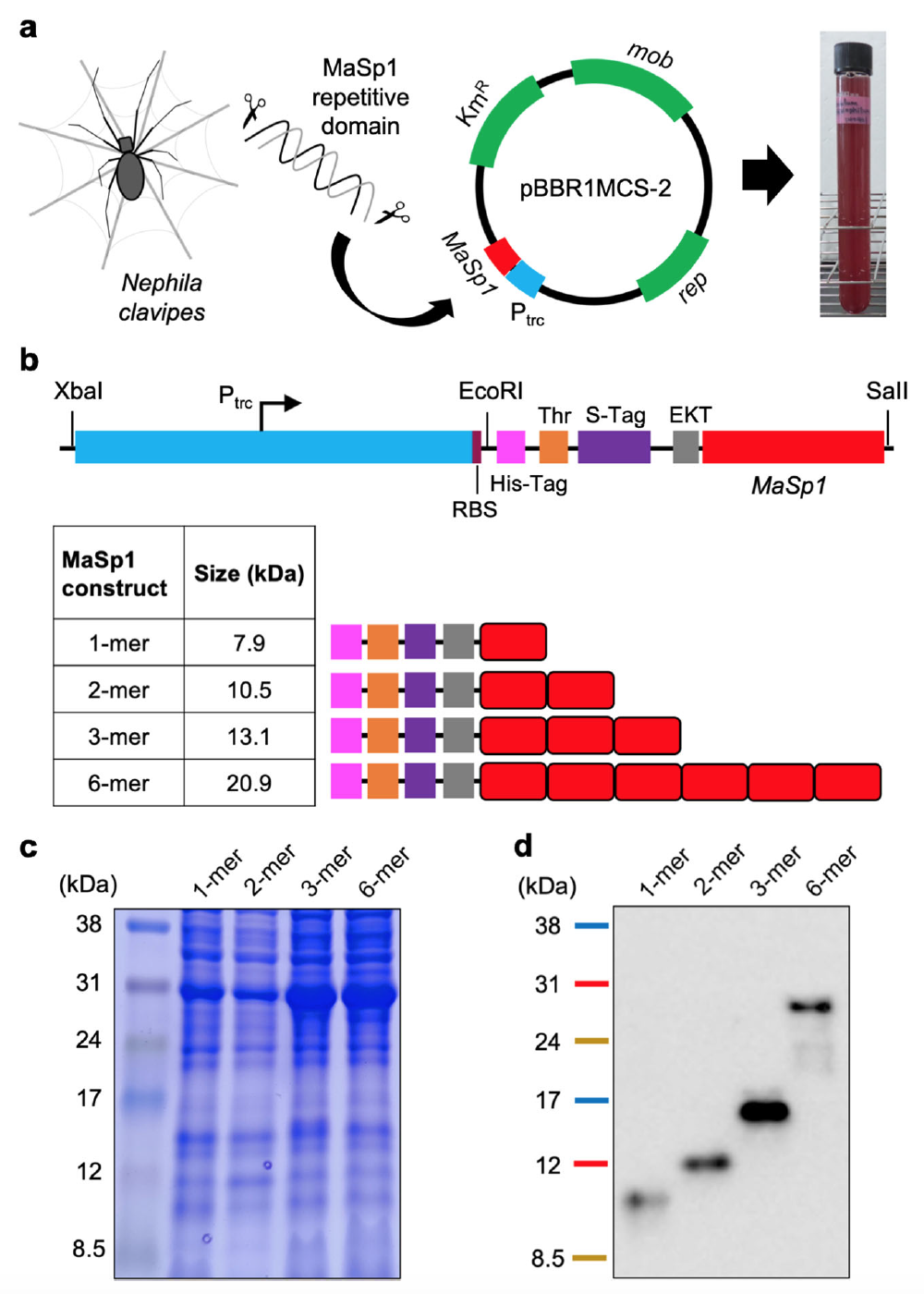
Изображение №1
Несмотря на то, что избыточная экспрессия рекомбинантных белков MaSp1 не была четко обнаружена во всех рекомбинантных культурах R.sulfidophilum с помощью электрофореза белков в полиакриламидном геле / SDSPAGE (1c), методом белкового иммуноблота была подтверждена положительная экспрессия белков MaSp1 для всех созданных рекомбинантных клеток R.sulfidophilum, несущих pBBR1-Ptrc-MaSp1-(1-мер, 2-мер, 3-мер или 6-мер) (1d).
К-меры* — подпоследовательности длиной k, содержащиеся в биологической последовательности.Единственный повторяющийся домен в полученных конструкциях содержит 33 аминокислотных остатка следующего вида:
NH2-SGRGGLGGQGAGAAAAAGGAGQGGYGGLGSQGT-COOH.
Теоретическая молекулярная масса белков-мишеней, включая неспидроиновые последовательности (области расщепления His-Tag, S-Tag, энтерокиназы и тромбина) на N-конце составляет 7.9 кДа для 1-мера (81 аа); 10.5 кДа для 2-мера (114 ак); 13.1 кДа для 3-мера (147 ак) и 20.9 кДа для 6-мера (246 ак.).
Да — обозначение Атомной единицы массы; кДа — килодальтон (1 кДа = 103 Да).В дополнение к подтверждению экспрессии белков MaSp1, была также проведена оценка их количества белков MaSp1, полученных из рекомбинантных культур R.sulfidophilum: ~ 3–10 мг/л (1-мер = 3.4 мг/л; 2-мер = 3.9 мг/л; 3-мер = 10.2 мг/л; 6-мер = 6.8 мг/л) или 3.5–6.9 % от общего количества белков. Для сравнения, гетерологичная экспрессия спидроинов в хорошо известной и широко используемой рекомбинантной системе E.coli способна продуцировать лишь ~ 0.3–1.2 мг/л очищенного спидроина.
Доминирующий аллель обозначается заглавной буквой (A против a). Поскольку каждый родитель предоставляет один аллель, возможны следующие комбинации: AA, Aa и aa.
Самым удивительным результатом, по словам ученых, в данном исследовании является демонстрация фабрик микробных клеток, основанных на морских фотосинтезирующих организмах, в которых можно применять режим фотоавтотрофного роста с использованием возобновляемого непищевого сырья и морской воды в качестве среды для культивирования.
R.sulfidophilum, несущий pBBR1-Ptrc-MaSp1-(6-мер), был культивирован в искусственной морской воде (Daigo ASW от artificial seawater) при освещении светодиодами (730 нм, 20–30 Вт/м2) с бикарбонатной солью (1 г/л) в качестве источника неорганического углерода и газообразным азотом (0.5 л/д) в качестве источника азота. Продолжительность культивирования составила 7 дней (2а).

Изображение №2
Крупнейшее составное звено MaSp1-(6-мер) было выбрано для последующих экспериментов, потому что более высокая молекулярная масса MaSp1 привела бы к большей прочности на растяжение волокна шелка паука. Бикарбонат натрия использовался для подачи неорганического углерода, поскольку бикарбонатные соли обладают большей растворимостью и более низкими расходами на транспортировку, чем газообразный CO2.
Ранее ученые уже проводили эксперименты для определения необходимых условий освещения для роста клеток R.sulfidophilum: интенсивность (8 и 50 Вт/м2) и длина волны (730, 800 и 850 нм). В этом исследовании была проведена оценка влияния на рост рекомбинантной R.sulfidophilum нескольких дополнительных питательных веществ (дрожжевой экстракт, витамин, железо и фосфор), которые испытывают дефицит в среде ASW.
Сухая клеточная масса (CDM) уменьшилась с 0.90 г/л (со всеми питательными веществами) до 0.66 г/л в отсутствие дрожжевого экстракта и до 0.39 г/л в отсутствие фосфора. Также было определено, что рекомбинантная R.sulfidophilum не может расти в среде ASW без подачи NaHCO3, газа N2 или фосфора (2b; ASW + N2, ASW + C + N2, ASW + C + P, and ASW + P + N2).
CDM (~ 0.4 г/л) в таких вариантах ASW среды, вероятнее всего, произошла из инокулянтов* или посевных культур даже после того, как образцы были промыты 2% хлоридом натрия. Таким образом, источники углерода, азота и фосфора необходимы для роста рекомбинантной R.sulfidophilum в среде ASW.
Микробиологический инокулянт* — биопрепараты, содержащие живые культуры микроорганизмов, полезных для растений.Как и ожидалось, рост клеток значительно увеличился с 0.34 ± 0.02 г/л (ASW + C + N2) до 0.58 ± 0.08 г/л (увеличение в 1.7 раза) и до 0.81 ± 0.02 г/л (увеличение в 2.4 раза) в присутствии дрожжевого экстракта (ASW + C + N2 + YE) и фосфора (ASW + C + N2 + P) соответственно.
Наивысший CDM был достигнут путем добавления дрожжевого экстракта и фосфора, что дало 1.04 ± 0.06 г/л (увеличение в 3.1 раза).
Выход ~ 0.2 мг/л рекомбинантного белка MaSp1 (2% от общего количества белков), наблюдался в условиях ASW + N2, ASW + C + N2, ASW + C + P и ASW + P + N2 (2c и 2d). Продуцированию белка MaSp1 способствовало добавление дрожжевого экстракта, который значительно увеличивал выход белка MaSp1 с 0.12 ± 0.10 мг/л (ASW + C + N2) до 3.93 ± 2.76 мг/л (ASW + C + YE + N2).
Добавление дрожжей также увеличило процентное содержание MaSp1 в общем объеме белков с 1.2 ± 1.0 до 6.9 ± 5.3%. Любопытно, что добавление фосфора хоть и положительно влияло на увеличение CDM, но негативно влияло на выработку белка MaSp1.
По сравнению с ASW + C + YE + N2 в варианте среды ASW + C + YE + P + N2 выход белка MaSp1 снизился до 2.71 ± 1.09 мг/л, а процентное содержание MaSp1 в общих белках до 3.9 ± 1.6%.
Объяснением этих разностей в выработке белка в зависимости от среды культивирования может заключаться в функционале каждого из компонентов. Например, дрожжевой экстракт в основном является источником азота, который способствует биосинтезу белка. Между тем, фосфор является важным макроэлементом и гетероэлементом во многих важных клеточных соединениях, что способствует росту первичных продуцентов.
Для получения паучьего шелка в его привычном виде, необходимо было провести очистку MaSp1.

Изображение №3
Чтобы получить достаточное количество белка MaSp1 для экструзии волокна, была проведена ферментация (3а) для производства MaSp1-(6-мер).
В целом, размеры спидроинов имеют положительную корреляцию с пределом прочности при растяжении до определенного размера молекулярной массы. Большие белки обладают большим количеством межцепочечных и внутрицепочечных взаимодействий, большим количеством запутываний и меньшим количеством дефектов на конце цепи.
Очищение MaSp1-(6-мер) проводили с использованием аффинной хроматографии через гистидиновую метку, которая присутствовала на N-конце генной кассеты MaSp1, и гель-фильтрационной хроматографией. В результате было получено ~ 10 мг очищенного MaSp1-(6-мер) (3b) из ~ 40 г CWM.
Шелковые волокна получали путем пипетирования 10 мас.% очищенного MaSp1-(6 мера), растворенного в гексафторизопропаноле (HFIP), в коагуляционную ванну с последующим ручным вытягиванием щипцами (3c). Наилучшие результаты были получены при использовании 90% 2-пропанола в качестве коагуляционной ванны, что вызывало относительно мягкое обезвоживание, что позволило эффективно вытягивать нити. Анализ с помощью сканирующей электронной микроскопии показал, что волокна имеют диаметр 10–20 мкм и поверхность, покрытую бороздками, параллельными оси волокна. Фрактография показала, что внутренняя структура состояла из микрофибрилл (3d и 3е).
Для более детального ознакомления с нюансами исследования рекомендую заглянуть в доклад ученых и дополнительные материалы к нему.
Эпилог
В данном труде ученые рассказали об успешном создании микро-фабрики по производству белка MaSp1. Основным передовиком этого производства является бактерия R.sulfidophilum, благодаря которой удалось достичь фотогетеротрофной экспрессии искусственного белка паутины в условиях фотоавтотрофного роста.
Другими словами, ученые генетически модифицировали бактерию для производства паучьего шелка, а точнее белка MaSp1, который является важной его составляющей. Помимо генетических манипуляций также необходимо было установить оптимальные условия культивации бактерии. Как оказалось, идеальной средой является искусственная морская вода. Дополнительно необходимо было использовать газообразный азот и дрожжевой экстракт в качестве источников питательных веществ. В совокупности эти составляющие приводят к эффективному росту бактерии и, следовательно, производству белка паутины.
Важно и то, что полученные из белка волокна паутины по своей структуре очень сильно напоминают натуральные, производимые пауками вида Nephila.
Ученые отмечают, что их метод выращивания белка паучьего шелка может быть использован и для выращивания других веществ. В дальнейшем авторы исследования планируют усовершенствовать свою микро-фабрику для повышения объемов производства белка и улучшения молекулярных характеристик результирующего продукта.
По мнению ученых, их труд может поспособствовать в решении многих проблем: энергетический, водный и продовольственный кризисы, проблемы с твердыми отходами, глобальное потепление и т.д. Причиной такого широкого спектра возможностей является факт того, что подобные фабрики производят биоразлагаемые и биосовместимые материалы с помощью углеродно-нейтрального процесса.
Благодарю за внимание, оставайтесь любопытствующими и хорошей всем рабочей недели, ребята. :)
Немного рекламы
Спасибо, что остаётесь с нами. Вам нравятся наши статьи? Хотите видеть больше интересных материалов? Поддержите нас, оформив заказ или порекомендовав знакомым, облачные VPS для разработчиков от $4.99, уникальный аналог entry-level серверов, который был придуман нами для Вас: Вся правда о VPS (KVM) E5-2697 v3 (6 Cores) 10GB DDR4 480GB SSD 1Gbps от $19 или как правильно делить сервер? (доступны варианты с RAID1 и RAID10, до 24 ядер и до 40GB DDR4).
Dell R730xd в 2 раза дешевле в дата-центре Equinix Tier IV в Амстердаме? Только у нас 2 х Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 ТВ от $199 в Нидерландах! Dell R420 — 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB — от $99! Читайте о том Как построить инфраструктуру корп. класса c применением серверов Dell R730xd Е5-2650 v4 стоимостью 9000 евро за копейки?
