(ответ биолога на статью «Вы неправильно пишете животных»)

В каждой клетке есть тысячи генов. Никогда не бывает так, чтобы они все работали одновременно. Клетки мышц, печени и мозга несут одинаковый набор генов. Они такие разные, потому что в них работают разные гены. Все клетки умеют включать и выключать отдельные гены в ответ на разные внешние воздействия. То есть система, которая управляет активностью генов — это такая система автоматического управления. Ученые хотят понимать, как такая автоматика работает, чтобы уметь ее чинить и взламывать. Например, в клетках человека есть система из примерно трехсот генов и белков, которая управляет делением клетки. Когда она ломается и клетка начинает все время делиться, возникает рак.

Упрощенная схема генной сети, регулирующей деление клеток человека
В «железе» обычно используются электрические импульсы. Сигналы в биологии, как правило, химические, то есть изменения концентрации каких-нибудь веществ. В нервной системе есть электрические сигналы, но это только приспособление к быстрой дальней передаче, подобно оптоволокну в технике. Передача нервного импульса от клетки к клетке происходит в химической форме, долговременная память и сложная интеграция сигналов в нейроне тоже химическая.
Где есть сигналы, там будут наводки — сигналы не на своем месте и шумы — случайная фигня, прилипающая к сигналам. В электронике приход сигналов по адресу обеспечивается проводами и изоляцией. Наводки возникают из-за паразитных емкостных и индуктивных связей между проводниками. В клетке бактерии ее содержимое более-менее равномерно перемешано, и любой химический сигнал (а их тысячи) доступен в любой ее точке. Клетки животных и растений разделены на отсеки с разным химическим составом, но типов этих отсеков меньше десятка и в каждом есть сотни и тысячи разных веществ.
Приход сигнала в нужное место клетки происходит благодаря молекулярному узнаванию по принципу «ключ-замок». Одна молекула белка может узнавать другой белок, белок может узнавать определенную последовательность ДНК, белок может узнавать маленькие молекулы, такие как сахара. Это узнавание не всегда идеально точное, поэтому молекулы, похожие по форме на штатного партнера по узнаванию, будут создавать наводки. Кроме наводок, в электронике есть шумы. Они возникают из-за теплового движения атомов, которое вносит долю хаоса в движение электронов. В клетке химические шумы тоже связаны с тепловым движением. Когда сигнал слабый, например, десять штук молекул данного типа на всю клетку, эти молекулы будут разбросаны по клетке случайно, и не факт, что равномерно. В результате их концентрация в каком-то углу клетки будет случайно колебаться, и это будет шум.
Клетку можно рассматривать как завод, который производит все необходимое ему оборудование и может собирать из него второй такой же завод. Основным оборудованием являются рибосомы — станки с ЧПУ, собирающие все белки. Структура собираемого белка записана на ленте — матричной РНК (мРНК). Рибосома движется по мРНК и по ее инструкции собирает цепочку нового белка из отдельных звеньев — аминокислот. Выходящая из рибосомы белковая цепочка сворачивается в компактный клубок зрелого белка, который начинает работать. Белки могут ускорять химические реакции (ферменты), а так же заниматься транспортом веществ, передачей сигналов, защитой и многими другими делами.

мРНК образуются как копии отдельных участков клеточной ДНК. ДНК можно сравнить с архивом технологической документации в кабинете главного инженера, а мРНК — с копиями чертежей, которые выдаются в цех. Копировальный аппарат, создающий эти копии — это тоже белок, который называется РНК-полимераза. Она может садиться на ДНК и начинать ее копирование не везде, а только на специальных участках ДНК — промоторах, которые находятся перед каждым геном или группой работающих вместе генов.
Включение и выключение генов определяется в основном на этапе посадки РНК-полимеразы на промотор. Если РНК-полимераза легко садится на промотор гена, то с него делается много мРНК-копий и рибосомы производят много молекул белка, кодируемого этим геном — он будет включен. Если что-то помешает посадке РНК-полимеразы, то ген окажется выключен. То есть, включение и выключение генов происходит на этапе взаимодействия РНК-полимеразы и промотора. Различные другие молекулы могут помогать или мешать их связыванию. Эти другие молекулы, в первую очередь специальные регуляторные белки, вместе с промотором и соседними участками ДНК образуют логический элемент, который может интегрировать несколько разных входных сигналов.
Пожалуй, самый изученный пример генного переключателя — лактозный оперон кишечной палочки. Французы Жакоб и Моно за его исследования были удостоены Нобелевской премии в 1965 году. Кишечная палочка, как понятно из ее названия, живет в кишечнике. Это может быть кишечник самых разных животных, от пчелы до человека. Ей там приходится питаться тем, что попалось хозяину, поэтому она может есть много разных питательных веществ.

Кишечная палочка под микроскопом и на чашке Петри
Кишечная палочка может расти, например, на питательной среде, состоящей только из глюкозы и минеральных солей и производить все необходимые ей аминокислоты и витамины. Вместо глюкозы могут быть и другие сахара (фруктоза, солодовый сахар — мальтоза, молочный сахар — лактоза и десяток других), а так же полисахариды, например крахмал.
Для усвоения каждого из этих сахаров нужны свои ферменты. Производство этих ферментов стоит запускать, только когда соответствующий сахар есть в среде, иначе материалы и энергия на производство этих ферментов будут потрачены зря. То есть, гены этих ферментов усвоения сахаров должны включаться только когда есть этот сахар. Для усвоения каждого сахара нужно, как правило, несколько ферментов, а не один. Их гены находятся в цепи ДНК рядом и их активность управляется одним общим регуляторным участком ДНК в начале первого гена. Такая группа совместно работающих и синхронно управляемых генов называется «оперон».
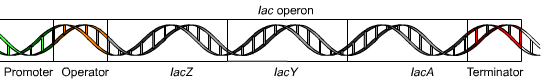
Схема лактозного оперона
Лактозный оперон состоит из трех генов. Первый (LacZ) кодирует транспортный белок, накачивающий лактозу в клетку, а два других (LacI и LacA) — ферменты, совместная работа которых превращает лактозу в «дефолт-сахар» — глюкозу. В начале лактозного оперона находится участок связывания РНК-полимеразы (промотор) и участок связывания регуляторных белков (оператор).
Активность лактозного оперона управляется двумя сигналами. Первый сигнал, это, очевидно, концентрация лактозы. Если лактозы нет, то и ферменты ее усвоения не нужны. Второй сигнал чуть сложнее. В одном из экспериментов Жакоб и Моно растили кишечную палочку на среде, содержащей и лактозу, и с глюкозу. В таких условиях палочка сначала потребляет глюкозу, а лактозный оперон у нее выключен. Когда глюкоза кончается, рост бактерий приостанавливается минут на 15-20, а затем продолжается уже за счет лактозы. Во время паузы лактозный оперон включается. То есть, второй регуляторный вход выключает лактозный оперон, когда у клетки есть более доступные сахара, чем лактоза (усвоение глюкозы не требует никаких дополнительных ферментов).
Дальнейшие эксперименты показали, что лактозный оперон не реагирует на саму глюкозу. Вместо этого внутри клетки кишечной палочки уровень голода (точнее, «вкусность» доступных сахаров) кодируется специальным сигнальным веществом. Оно называется «циклический аденозин-монофосфат», или цАМФ. Пока палочка растет на глюкозе, цАМФ в клетке практически нет. Если нет глюкозы, но есть мальтоза или крахмал (чуть более трудноусвояемые вещества), вырабатывается немного цАМФ. Если нет мальтозы, но есть фруктоза или лактоза, уровень цАМФ в клетке будет выше. Если нет никаких сахаров, но есть молочная кислота — еще выше, и наконец, если ничего вкусного нет и приходится жрать глицерин, то уровень цАМФ будет самым высоким. Итак, лактозным опероном управляют два сигнала: концентрация лактозы и концентрация цАМФ.
Как эти сигналы действуют на активность генов? Активный ген — это такой, на котором РНК-полимераза производит много матричных РНК. РНК-полимераза начинает работу над данным опероном всегда с посадки на один и тот же участок ДНК (он называется «промотор»). Где там место для лактозы и цАМФ? РНК-полимераза не может распознавать все те сотни сигналов, которые регулируют активность тысяч генов. Для этого существуют специальные регуляторные белки (они называются «транскрипционные факторы»). В управлении лактозным опероном участвуют два регуляторных белка, по одному на каждый входной сигнал: лактозный репрессор и катаболический активатор.

Лактозный репрессор (фиолетовый) на ДНК
Лактозный репрессор — это белок, который умеет связываться либо с лактозой, либо с определенной последовательностью ДНК. В геноме кишечной палочки есть две такие последовательности, обе в начале лактозного оперона, по обе стороны от промотора. Молекулы лактозного репрессора прочно слипаются друг с другом в группы по четыре белковых молекулы. Связывание такой четверки с ДНК закручивает нить ДНК в крутую петлю, в которой оказывается промотор. РНК-полимераза не может сесть на такой закрученный промотор и ген оказывается выключен. Если в клетке появляется лактоза, она связывается с лактозным репрессором и он отваливается от ДНК, освобождая промотор для РНК-полимеразы — оперон начинает работать. Так устроен регуляторный вход оперона по концентрации лактозы.
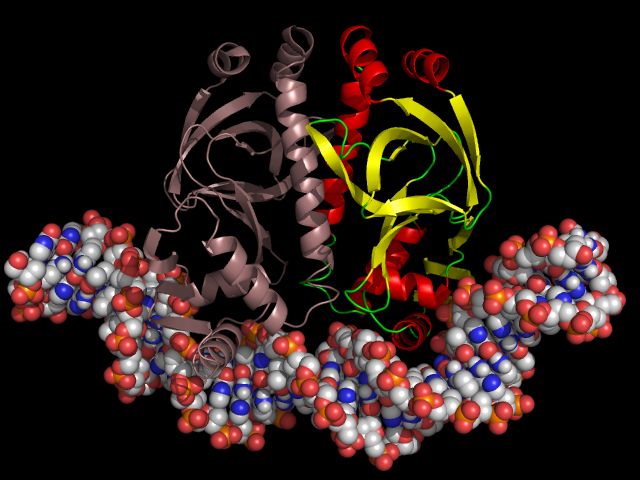
Катаболический активатор на ДНК
Катаболический активатор похожим способом реагирует на концентрацию цАМФ. Правда, есть несколько отличий в деталях:
— катаболический активатор садится на ДНК чуть сбоку от промотора и не перекрывает его. Наоборот, он усиливает связывание РНК-полимеразы с промотором и повышает активность оперона.
— катаболический активатор связывает цАМФ и ДНК. Без цАМФ он не может связаться с ДНК.
— катаболический активатор нужен для полной активности лактозного оперона, но и без него оперон все же будет работать примерно на 5% от полной активности. Лактозный репрессор же регулирует оперон в диапазоне от 0 до 100%.
— молекулы катаболического активатора соединяются в пары, а не в четверки. В следующем посте мы увидим, к чему приводит эта разница.
То есть, мы можем написать таблицу истинности для лактозного оперона:
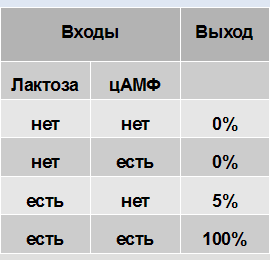
Лактозный оперон работает почти как логический элемент AND. Только 5% активности в состоянии «лактоза+, цАМФ — » слегка выпадают из идеальной картины.
Продолжение с графиками и матаном: https://geektimes.ru/post/283686/

В каждой клетке есть тысячи генов. Никогда не бывает так, чтобы они все работали одновременно. Клетки мышц, печени и мозга несут одинаковый набор генов. Они такие разные, потому что в них работают разные гены. Все клетки умеют включать и выключать отдельные гены в ответ на разные внешние воздействия. То есть система, которая управляет активностью генов — это такая система автоматического управления. Ученые хотят понимать, как такая автоматика работает, чтобы уметь ее чинить и взламывать. Например, в клетках человека есть система из примерно трехсот генов и белков, которая управляет делением клетки. Когда она ломается и клетка начинает все время делиться, возникает рак.

Упрощенная схема генной сети, регулирующей деление клеток человека
Как устроена внутриклеточная автоматика?
В «железе» обычно используются электрические импульсы. Сигналы в биологии, как правило, химические, то есть изменения концентрации каких-нибудь веществ. В нервной системе есть электрические сигналы, но это только приспособление к быстрой дальней передаче, подобно оптоволокну в технике. Передача нервного импульса от клетки к клетке происходит в химической форме, долговременная память и сложная интеграция сигналов в нейроне тоже химическая.
Где есть сигналы, там будут наводки — сигналы не на своем месте и шумы — случайная фигня, прилипающая к сигналам. В электронике приход сигналов по адресу обеспечивается проводами и изоляцией. Наводки возникают из-за паразитных емкостных и индуктивных связей между проводниками. В клетке бактерии ее содержимое более-менее равномерно перемешано, и любой химический сигнал (а их тысячи) доступен в любой ее точке. Клетки животных и растений разделены на отсеки с разным химическим составом, но типов этих отсеков меньше десятка и в каждом есть сотни и тысячи разных веществ.
Приход сигнала в нужное место клетки происходит благодаря молекулярному узнаванию по принципу «ключ-замок». Одна молекула белка может узнавать другой белок, белок может узнавать определенную последовательность ДНК, белок может узнавать маленькие молекулы, такие как сахара. Это узнавание не всегда идеально точное, поэтому молекулы, похожие по форме на штатного партнера по узнаванию, будут создавать наводки. Кроме наводок, в электронике есть шумы. Они возникают из-за теплового движения атомов, которое вносит долю хаоса в движение электронов. В клетке химические шумы тоже связаны с тепловым движением. Когда сигнал слабый, например, десять штук молекул данного типа на всю клетку, эти молекулы будут разбросаны по клетке случайно, и не факт, что равномерно. В результате их концентрация в каком-то углу клетки будет случайно колебаться, и это будет шум.
Что конкретно регулируется в живой клетке?
Клетку можно рассматривать как завод, который производит все необходимое ему оборудование и может собирать из него второй такой же завод. Основным оборудованием являются рибосомы — станки с ЧПУ, собирающие все белки. Структура собираемого белка записана на ленте — матричной РНК (мРНК). Рибосома движется по мРНК и по ее инструкции собирает цепочку нового белка из отдельных звеньев — аминокислот. Выходящая из рибосомы белковая цепочка сворачивается в компактный клубок зрелого белка, который начинает работать. Белки могут ускорять химические реакции (ферменты), а так же заниматься транспортом веществ, передачей сигналов, защитой и многими другими делами.

мРНК образуются как копии отдельных участков клеточной ДНК. ДНК можно сравнить с архивом технологической документации в кабинете главного инженера, а мРНК — с копиями чертежей, которые выдаются в цех. Копировальный аппарат, создающий эти копии — это тоже белок, который называется РНК-полимераза. Она может садиться на ДНК и начинать ее копирование не везде, а только на специальных участках ДНК — промоторах, которые находятся перед каждым геном или группой работающих вместе генов.
Включение и выключение генов определяется в основном на этапе посадки РНК-полимеразы на промотор. Если РНК-полимераза легко садится на промотор гена, то с него делается много мРНК-копий и рибосомы производят много молекул белка, кодируемого этим геном — он будет включен. Если что-то помешает посадке РНК-полимеразы, то ген окажется выключен. То есть, включение и выключение генов происходит на этапе взаимодействия РНК-полимеразы и промотора. Различные другие молекулы могут помогать или мешать их связыванию. Эти другие молекулы, в первую очередь специальные регуляторные белки, вместе с промотором и соседними участками ДНК образуют логический элемент, который может интегрировать несколько разных входных сигналов.
Логические элементы на ДНК и белках
Пожалуй, самый изученный пример генного переключателя — лактозный оперон кишечной палочки. Французы Жакоб и Моно за его исследования были удостоены Нобелевской премии в 1965 году. Кишечная палочка, как понятно из ее названия, живет в кишечнике. Это может быть кишечник самых разных животных, от пчелы до человека. Ей там приходится питаться тем, что попалось хозяину, поэтому она может есть много разных питательных веществ.

Кишечная палочка под микроскопом и на чашке Петри
Кишечная палочка может расти, например, на питательной среде, состоящей только из глюкозы и минеральных солей и производить все необходимые ей аминокислоты и витамины. Вместо глюкозы могут быть и другие сахара (фруктоза, солодовый сахар — мальтоза, молочный сахар — лактоза и десяток других), а так же полисахариды, например крахмал.
Для усвоения каждого из этих сахаров нужны свои ферменты. Производство этих ферментов стоит запускать, только когда соответствующий сахар есть в среде, иначе материалы и энергия на производство этих ферментов будут потрачены зря. То есть, гены этих ферментов усвоения сахаров должны включаться только когда есть этот сахар. Для усвоения каждого сахара нужно, как правило, несколько ферментов, а не один. Их гены находятся в цепи ДНК рядом и их активность управляется одним общим регуляторным участком ДНК в начале первого гена. Такая группа совместно работающих и синхронно управляемых генов называется «оперон».

Схема лактозного оперона
Лактозный оперон состоит из трех генов. Первый (LacZ) кодирует транспортный белок, накачивающий лактозу в клетку, а два других (LacI и LacA) — ферменты, совместная работа которых превращает лактозу в «дефолт-сахар» — глюкозу. В начале лактозного оперона находится участок связывания РНК-полимеразы (промотор) и участок связывания регуляторных белков (оператор).
Активность лактозного оперона управляется двумя сигналами. Первый сигнал, это, очевидно, концентрация лактозы. Если лактозы нет, то и ферменты ее усвоения не нужны. Второй сигнал чуть сложнее. В одном из экспериментов Жакоб и Моно растили кишечную палочку на среде, содержащей и лактозу, и с глюкозу. В таких условиях палочка сначала потребляет глюкозу, а лактозный оперон у нее выключен. Когда глюкоза кончается, рост бактерий приостанавливается минут на 15-20, а затем продолжается уже за счет лактозы. Во время паузы лактозный оперон включается. То есть, второй регуляторный вход выключает лактозный оперон, когда у клетки есть более доступные сахара, чем лактоза (усвоение глюкозы не требует никаких дополнительных ферментов).
Дальнейшие эксперименты показали, что лактозный оперон не реагирует на саму глюкозу. Вместо этого внутри клетки кишечной палочки уровень голода (точнее, «вкусность» доступных сахаров) кодируется специальным сигнальным веществом. Оно называется «циклический аденозин-монофосфат», или цАМФ. Пока палочка растет на глюкозе, цАМФ в клетке практически нет. Если нет глюкозы, но есть мальтоза или крахмал (чуть более трудноусвояемые вещества), вырабатывается немного цАМФ. Если нет мальтозы, но есть фруктоза или лактоза, уровень цАМФ в клетке будет выше. Если нет никаких сахаров, но есть молочная кислота — еще выше, и наконец, если ничего вкусного нет и приходится жрать глицерин, то уровень цАМФ будет самым высоким. Итак, лактозным опероном управляют два сигнала: концентрация лактозы и концентрация цАМФ.
Как эти сигналы действуют на активность генов? Активный ген — это такой, на котором РНК-полимераза производит много матричных РНК. РНК-полимераза начинает работу над данным опероном всегда с посадки на один и тот же участок ДНК (он называется «промотор»). Где там место для лактозы и цАМФ? РНК-полимераза не может распознавать все те сотни сигналов, которые регулируют активность тысяч генов. Для этого существуют специальные регуляторные белки (они называются «транскрипционные факторы»). В управлении лактозным опероном участвуют два регуляторных белка, по одному на каждый входной сигнал: лактозный репрессор и катаболический активатор.
Лактозный репрессор (фиолетовый) на ДНК
Лактозный репрессор — это белок, который умеет связываться либо с лактозой, либо с определенной последовательностью ДНК. В геноме кишечной палочки есть две такие последовательности, обе в начале лактозного оперона, по обе стороны от промотора. Молекулы лактозного репрессора прочно слипаются друг с другом в группы по четыре белковых молекулы. Связывание такой четверки с ДНК закручивает нить ДНК в крутую петлю, в которой оказывается промотор. РНК-полимераза не может сесть на такой закрученный промотор и ген оказывается выключен. Если в клетке появляется лактоза, она связывается с лактозным репрессором и он отваливается от ДНК, освобождая промотор для РНК-полимеразы — оперон начинает работать. Так устроен регуляторный вход оперона по концентрации лактозы.

Катаболический активатор на ДНК
Катаболический активатор похожим способом реагирует на концентрацию цАМФ. Правда, есть несколько отличий в деталях:
— катаболический активатор садится на ДНК чуть сбоку от промотора и не перекрывает его. Наоборот, он усиливает связывание РНК-полимеразы с промотором и повышает активность оперона.
— катаболический активатор связывает цАМФ и ДНК. Без цАМФ он не может связаться с ДНК.
— катаболический активатор нужен для полной активности лактозного оперона, но и без него оперон все же будет работать примерно на 5% от полной активности. Лактозный репрессор же регулирует оперон в диапазоне от 0 до 100%.
— молекулы катаболического активатора соединяются в пары, а не в четверки. В следующем посте мы увидим, к чему приводит эта разница.
То есть, мы можем написать таблицу истинности для лактозного оперона:

Лактозный оперон работает почти как логический элемент AND. Только 5% активности в состоянии «лактоза+, цАМФ — » слегка выпадают из идеальной картины.
Продолжение с графиками и матаном: https://geektimes.ru/post/283686/
