Что такое клинический алгоритм
В медицине существуют подробные правила диагностики и лечения больных, которые выражают последовательность действий и решений врача. Эти правила воплощены в алгоритмах.
Клинический алгоритм есть пошаговое описание действий врача при решении лечебно-диагностических задач и вопросов врачебной практики.
Кто разрабатывает клинические алгоритмы? Профессиональные врачи, т. е. специалисты, имеющие высшее медицинское образование и опыт диагностики и лечения.
Профессор И. В. Коробко из Минздрава РФ отмечает:
«Применение клинических алгоритмов имеет давние традиции как для составления клинических рекомендаций и руководств, так и для практической медицинской деятельности».
История вопроса

По языку ДРАКОН на Хабре опубликованы около десяти статей, по медицинскому языку ДРАКОН — две статьи:
Подробнее о медицинском языке ДРАКОН см. здесь.
Существующие клинические рекомендации по COVID-19 описывают алгоритмы лечения в виде обычного текста, причем некоторые шаги алгоритма пропущены (отсутствуют). Это важный недостаток.
Медицинский язык ДРАКОН позволяет устранить недочет и описать клинические алгоритмы в виде чертежей высокой точности. Преимущество графики в том, что эргономичную (user-friendly) медицинскую "картинку" легче понять, чем сложный медицинский текст.

Пришла пора сделать следующий шаг
Я пригласил в соавторы десять опытных врачей и мы общими усилиями подготовили учебное пособие: «Клиническая алгоритмическая медицина. Алгоритмы диагностики и лечения на медицинском языке ДРАКОН. / Сморкалов А. Ю., Бочанова Е. Н. и др. – 477 с. – Иллюстраций: 200».
В книге, в частности, разработаны и описаны алгоритмы для лечения коронавирусной инфекции COVID-19. Под катом полный список авторов книги со всеми титулами.
Hidden text
Список авторов
Сморкалов Андрей Юрьевич, кандидат медицинских наук, доцент, врач анестезиолог-реаниматолог высшей категории. Место работы: [Cистемный интегратор обучения в медицине] ООО Синтомед, город Москва, преподаватель, специалист по симуляционному обучению.
Бочанова Елена Николевна, доктор медицинских наук, доцент кафедры фармакологии и фармацевтического консультирования Красноярского государственного медицинского университета имени профессора В. Ф. Войно-Ясенецкого.
Гусев Сергей Дмитриевич, кандидат медицинских наук, доцент кафедры медицинской кибернетики и информатики Красноярского государственного медицинского университета имени профессора В. Ф. Войно-Ясенецкого.
Дмитренко Диана Викторовна — доктор медицинских наук, профессор, заведующая кафедрой медицинской генетики и клинической нейрофизиологии Института последипломного образования Красноярского государственного медицинского университета имени профессора В. Ф. Войно-Ясенецкого.
Шнайдер Наталья Алексеевна — доктор медицинских наук, профессор, ведущий научный сотрудник отделения персонализированной психиатрии и неврологии Национального медицинского исследовательского центра психиатрии и неврологии имени. В. М. Бехтерева.
Насырова Регина Фаритовна — доктор медицинских наук, главный научный сотрудник, руководитель отделения персонализированной психиатрии и неврологии Национального медицинского исследовательского центра психиатрии и неврологии имени. В. М. Бехтерева.
Лозовская Марина Эдуардовна, доктор медицинских наук, профессор, заведующая кафедрой фтизиатрии Санкт-Петербургского государственного медицинского педиатрического университета.
Малышева Анастасия Юрьевна, клинический ординатор кафедры фтизиатрии Санкт-Петербургского государственного медицинского педиатрического университета.
Бармин Дмитрий Борисович, клинический ординатор кафедры фтизиатрии Санкт-Петербургского государственного медицинского педиатрического университета.
Васильева Елена Борисовна, кандидат медицинских наук, доцент кафедры фтизиатрии Санкт-Петербургского государственного медицинского педиатрического университета.
Паронджанов Владимир Даниелович, кандидат технических наук, старший научный сотрудник Научно-производственного центра автоматики и приборостроения имени академика Н. А. Пилюгина.
Митькин Степан Борисович, разработчик программного обеспечения медицинского алгоритмического языка ДРАКОН. Место работы: ProsessPilotene AS, Asker, Norway.
Смертоносная инфекция
Счет погибших от коронавирусной инфекции COVID-19 идет на миллионы. Борьба с этим злом потребовала от человечества чрезвычайных усилий: финансовых, организационных, научных. Потребовались не только новые методы вакцинации и лечения, но и новые формы сотрудничества медицины и ИТ-отрасли или, как говорят, новые формы цифровой трансформации медицины.
Последнее направление, в частности, включает в себя разработку новых медицинских знаний, которые воплощаются в новых сложных клинических алгоритмах. Разработку таких алгоритмов ведут врачи, специалисты в области респираторной терапии.
Опытные врачи, исследователи и ученые, работая на переднем крае науки, создают новое медицинское знание, новые методы диагностики и лечения, которые воплощаются в алгоритмах диагностики и лечения. Это очень сложная, кропотливая, трудоемкая, творческая работа.
Есть ли специальные инструменты, помогающие врачам, ученым и преподавателям придумывать и разрабатывать клинические алгоритмы? Есть ли инструменты, облегчающие творческий труд по созданию алгоритмов диагностики и лечения? Делающие труд творческих работников комфортным, продуктивным, защищенным от ошибок?
Увы, таких инструментов пока нет.
Между тем в эпоху цифровой медицины и новых требований к охране общественного здоровья с учетом пандемии COVID-19 нужда в подобных инструментах становится очень острой.
Клинические алгоритмы следует разрабатывать с помощью программы ДРАКОН-конструктор
Клинический алгоритм на языке ДРАКОН не стоит рисовать вручную (с помощью универсального графического редактора типа Visio, yEd и пр.). Получится медленно, неаккуратно и с ошибками. Следует непременно использовать ДРАКОН-конструктор. Будет намного быстрее и лучше.
Посмотрите анимацию, показывающую, как ДРАКОН- конструктор создает дракон-алгоритм
Рис. 1. На анимации желтыми кружками показаны валентные точки (точки ввода икон)
Иконы можно вводить только в валентные точки. Они служат для предотвращения ошибок.
Программа DrakonHub
Попробуйте бесплатный онлайн ДРАКОН-конструктор DrakonHub https://drakonhub.com/.
Вот инструкция https://bit.ly/2Je1uHd.
Вы убедитесь, что процесс рисования алгоритма происходит удобно, легко и с большой скоростью.
Забудьте о линиях! Во избежание ошибок пользователю запрещено рисовать соединительные линии между иконами на дракон-схеме. Все соединительные линии автоматически создает программа ДРАКОН-конструктор.
Как работает ДРАКОН-конструктор
Ответ дает замедленная анимация на рис. 2.

Рис. 2. ДРАКОН-конструктор позволяет нарисовать сложный алгоритм в наглядном виде и очень быстро
Наглядно показаны действия пользователя по созданию алгоритма. Слева панель инструментов (тулбар, toolbar). Пользователь берет нужную фигуру из тулбара и вставляет ее в алгоритм.
На анимации видно, что пользователь не провел ни одной соединительной линии. Тем не менее все линии образовались, причем образовались правильно, без пересечений.
Следующая анимация поясняет, как переделать уже сделанный чертеж https://bit.ly/3rNgqhA.
Рис. 3. ДРАКОН-конструктор позволяет переделать уже сделанный чертеж алгоритма (удалять, вставлять и переставлять графические фигуры).
Рисунки 2 и 3 показывают работу с дракон-схемой примитив. Редактирование силуэта происходит точно так же. Переход от примитива к силуэту и обратно производится кнопкой на тулбаре внизу.
Достоинства редактора DrakonHub
Автоматическое появление валентных точек — мест возможной вставки икон выбранного типа — является преимуществом редактора DrakonHub. Это отличает его от Microsoft Visio, где элемент любого типа может быть помещен в любое место схемы.
Язык ДРАКОН содержит большое число правил. ДРАКОН-конструктор знает многие правила, хранит в своей памяти и скрупулезно выполняет их, облегчая тем самым труд пользователя и частично освобождая его от запоминания большого числа правил. Программа DrakonHub обеспечивает соблюдение правил построения дракон-схем и тем самым снижает вероятность ошибок.
Редактор помогает пользователю не только правильно добавлять в схему иконы, но и правильно их соединять — прокладывать маршруты клинического алгоритма.
Цель
Цель статьи — познакомить читателей с проблемой COVID-19. и респираторной терапией дыхательной недостаточности, ассоциированной с COVID-19.
Респираторная терапия — лечение, предназначенное для улучшения системы дыхания благодаря воздействию на аппарат вентиляции (лёгкие, грудная стенка и дыхательные мышцы).
В статье описаны четыре клинических алгоритма:
✅Низкочастотная оксигенация пациента.
✅Неинвазивная высокопоточная оксигенация пациента.
✅Аппаратная неинвазивная вентиляция легких.
✅Протективная искусственная вентиляция легких.
Что такое оксигенация
Оксигенация пациента (лечение кислородом) происходит, когда молекулы кислорода попадают в ткани организма. Кровь насыщается кислородом в легких, где молекулы кислорода перемещаются из воздуха в кровь.
Оксигенация крови — это уровень насыщения артериальной крови кислородом. Точнее, это процентное содержание в крови гемоглобина, насыщенного кислородом. Оксигенация обозначается SpO2, выражается количественно и измеряется с помощью пульсоксиметра. Это важный показатель состояния дыхательной системы человека. При уровне SpO2 ниже 90% повышается риск развития гипоксемии — дефицита кислорода в крови. Чем ниже показатель SpO2, тем выше риск.
Уроки пандемии COVID-19
Пандемия, вызванная распространением коронавируса SARS-CoV-2, — одна из самых смертоносных в истории человечества. По состоянию на апрель 2022 года заразились 500 миллионов человек, умерли свыше 6 миллионов. При осложнениях могут возникать острый респираторный дистресс-синдром (ОРДС) и пневмония (воспаление лёгких).
Органы власти во многих странах мира ввели жесткие ограничения на жизнь и работу людей: запретили путешествия, установили карантин на границах, ввели самоизоляцию и пр., что привело к сбоям в работе предприятий и нарушило цепочки поставок. Пандемия COVID-19 стала причиной серьёзных социально-экономических последствий, включая крупнейшую мировую рецессию после Великой депрессии.
Требования
Пандемия COVID-19 предъявила к медицинским учреждениям новые требования. С быстрым ростом числа COVID-заболеваний и ограниченностью коечного фонда в инфекционных клиниках потребовалось срочное перепрофилирование медучреждений под COVID-задачи и переобучение медперсонала для работы в красных зонах.
Возникла потребность обучения большого количества врачей различных специальностей методам оказания неотложной помощи при тяжелых и осложненных формах у пациентов с COVID-19 в условиях острого дефицита времени. В данной ситуации неоценимую роль играют алгоритмизация действий врача и методы симуляционного обучения.
Искусственная вентиляция легких
Проведение искусственной вентиляции легких (ИВЛ) у пациентов с COVID-19 является серьёзной проблемой для большинства врачей, не являющихся специалистами в области респираторной терапии.
Одной из основных трудностей проведения респираторной терапии пациентам с COVID-19 является отсутствие чётких алгоритмов и рекомендаций по выбору метода респираторной терапии и настройке аппаратов ИВЛ.
Чем опасна задержка
В свою очередь, увеличение количества пациентов с COVID-19, нуждающихся в интенсивной терапии с потенциальной потребностью в ИВЛ, привело к дефициту врачей, знающих принципы протективной вентиляции легких.
У пациентов с COVID-19 при позднем переводе на искусственную вентиляцию лёгких включается дополнительный повреждающий фактор – транспульмональное давление. Поэтому любая задержка перевода пациента на аппаратную вентиляцию лёгких приводит к увеличению объёма поражения лёгочной ткани.
В то же время сама ИВЛ является мощным повреждающим фактором, особенно при неправильно подобранных параметрах. Основными причинами этого повреждения становятся
волюмотравма,
баротравма,
циклическая травма,
оксигенотравма,
ателектотравма.
Хождение по лезвию ножа
Следовательно, подбор оптимальных параметров ИВЛ у больных с тяжёлыми вирусными пневмониями и острым респираторным дистресс-синдромом (ОРДС) — это своего рода «хождение по лезвию ножа».
Необходимо обеспечить минимально достаточный уровень оксигенации, при этом максимально снизив негативное влияние повреждающих факторов ИВЛ на лёгкие. По нашему опыту, даже незначительное отклонение на непродолжительное время от рамок протективной вентиляции приводит к дополнительному повреждению лёгких.
Важным фактором, влияющим на исход тяжелого вирусного поражения лёгких, является уровень подготовки врача отделения реанимации по особенностям проведения респираторной терапии указанным пациентам.
Алгоритмы респираторной терапии
С целью быстрого, качественного и доступного обучения специалистов, работающих в реанимации, нами были разработаны алгоритмы респираторной терапии при COVID -19. Алгоритмы основаны на следующих документах [1, 2, 3, 4, 5].
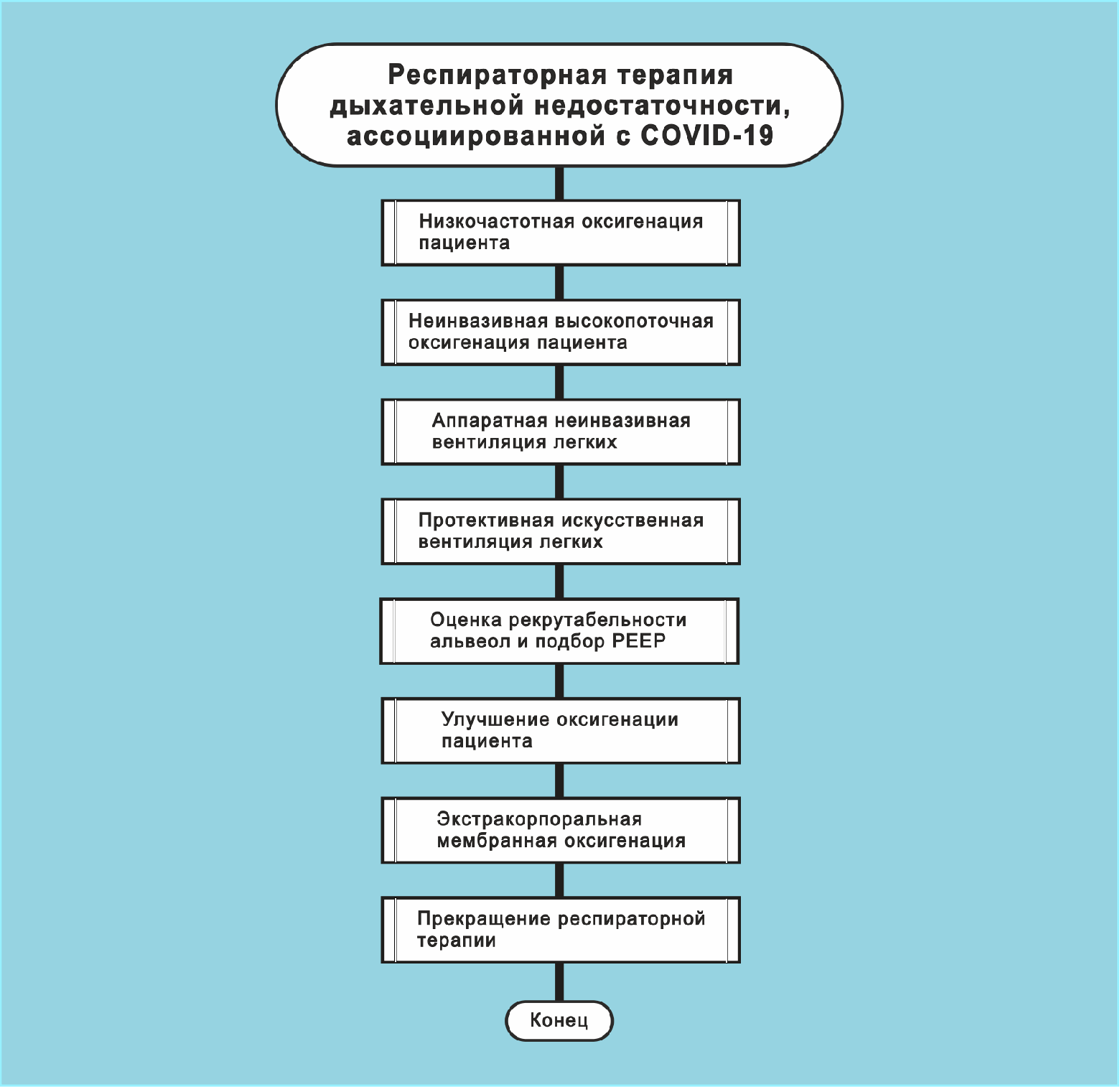
Рис. 4. Упрощенный алгоритм респираторной терапии.
В статье описаны верхние четыре алгоритма на рис. 4. Нижняя четверка алгоритмов будет представлена в следующей статье.
Общие сведения
Острая дыхательная недостаточность (ОДН) является одним из наиболее частых осложнений COVID-19. У пациентов с тяжелым и крайне тяжелым течением (10–15% случаев) после 5-го дня болезни сохраняется лихорадка, появляются симптомы дыхательной недостаточности, прогрессируют инфильтративные изменения в легких (вирусная пневмония), ОРДС.
Даже при легком течении COVID-19 у большинства пациентов при компьютерной томографии легких видны инфильтративные изменения. Коронавирус SARS-CoV-2 обнаруживался в носоглоточных смывах у 59% пациентов, а инфильтративные изменения на компьютерной томографии легких – у 88% пациентов с вероятным COVID-19.
Диффузное повреждение альвеол при COVID-19 диагностируют в среднем на 8-е сутки от начала болезни. При поступлении в отделение реанимации и интенсивной терапии частота ОРДС составляет около 60%, а индекс PaO2 / FiO2 – 136 (103–234 мм рт. ст).
При ОРДС у пациентов с COVID-19 высока частота гиперкапнии, сохраняющейся даже на фоне инвазивной ИВЛ из-за роста альвеолярного мертвого пространства (микротромбоз легочных капилляров, тромбоэмболия легочной артерии) и/или увеличения шунта (венозного примешивания). Это ведет к большой (выше 5 мм рт. ст.) разнице напряжений СО2 в артериальной крови и в конце выдоха.
Целевые показатели газообмена, ассоциированные с улучшением исхода при остром респираторном дистресс-синдроме:
PaO2 90–105 мм рт. ст. или SpO2 95-98%;
PaCO2 35–50 мм рт. ст., возможно допущение гиперкапнии до 70 мм рт. ст. при невозможности достижения нормокапнии при дыхательном объеме 6 мл/кг идеальной массы тела (ИМТ) и частоте дыхания 30 раз в минуту.
Алгоритм «Низкопоточная оксигенация пациента»

Рис. 5. Алгоритм «Низкопоточная оксигенация пациента».

Рис. 6. Названия икон языка ДРАКОН.
Все системы доставки кислорода в дыхательные пути пациента делят на:
низкопоточные (поток кислорода до 15 литров в минуту);
высокопоточные (поток кислорода 30–60 литров в минуту).
Самый простой алгоритм оказания помощи при острой дыхательной недостаточности изображен на рис. 5 — это низкопоточный вариант.
Необходимо иметь кислородный баллон или стационарную кислородную сеть. Кроме того, нужен интерфейс, через который кислород будет поступать в легкие пациента: назальные канюли, лицевая маска и т. д.
На рис. 5 слева показана первая ветка алгоритма, которая называется «Подготовка к низкопоточной оксигенации». Ветка имеет три выхода — три иконы Адрес:
Регулировка потока кислорода.
Высокопоточная оксигенация пациента.
Завершение.
В зависимости от условий, записанных в верхних иконах Вопрос, рабочая точка алгоритма будет перемещаться сверху вниз по маршрутам, ведущим к иконам Адрес.
При показателе SpO2 меньше 92% рекомендовано начать обычную оксигенотерапию (через лицевую маску или назальные канюли, лучше маску с расходным мешком) потоком до 15 литров в минуту до достижения SpO2 значения 96–98%.
Однако такой вариант годится не всем. Есть исключения.
Первое исключение
Если у больного нет дыхания, нет сознания и пр., его нужно сразу направить на другой алгоритм — «Протективную искусственную вентиляцию легких». На рис. 5 нарисован этот случай с помощью трех икон Вопрос:
Дыхание есть? Нет.
Сознание есть? Нет.
Есть ажитация или энцефалопатия? Да.
Во всех этих случаях через правый выход иконы Вопрос маршрут идет на вход иконы Вставка, обозначающей указанный алгоритм.
Второе исключение
Если у пациентов есть сопутствующие заболевания (хроническая обструктивная болезнь лёгких, хроническая сердечная недостаточность) больных следует сразу направлять на высокопоточный вариант.
Для этого через икону Адрес «Высокопоточная оксигенация пациента» переходим на рис. 5 на вход ветки с тем же названием. Затем попадаем в икону Вставка, обозначающую алгоритм «Неинвазивная высокопоточная оксигенация пациента». Оба алгоритма, обозначенные иконами Вставка, подробно раскрыты позже на рис. 97 и 100.
Низкопоточная оксигенация (продолжение)
Результирующая величина FiO2 зависит не только от потока кислорода, но и от состояния пациента. Следует принимать во внимание такие факторы, как минутная вентиляция и инспираторный поток пациента. Чем они больше, тем меньшая величина FiO2 получается в итоге.
Низкопоточная оксигенотерапия эффективна при легкой и средней степени тяжести гипоксемической острой дыхательной недостаточности. Имеется в виду индекс PaO2/FiO2, равный 300–150 мм рт. ст. (сатурация на воздухе без кислорода 75–93%).
Интерфейс низкопоточных систем можно расположить следующим образом в порядке повышения степени результирующей инспираторной фракции кислорода: носовые канюли → простые ороназальные маски → маски Вентури → ороназальные маски с резервуарным мешком.

Индекс оксигенации
У пациентов в критическом состоянии FiO2 используется для оценки способности легких к газообмену с применением соотношения PaO2/FiO2 (индекс оксигенации).
При этом степень острого респираторного дистресс-синдрома классифицируется согласно таблице.
Степень ОРДС | Индекс оксигенации |
Легкая | от 201 до 300 мм рт. ст. |
Средняя | от 101 до 200 мм рт. ст. |
Тяжелая | <100 мм рт. ст. |
Алгоритм «Неинвазивная высокопоточная оксигенация пациента»

Рис. 7. Алгоритм «Неинвазивная высокопоточная оксигенация пациента».
В алгоритме описан процесс перевода пациента на высокопоточную оксигенацию и подбора ее параметров (рис. 97).
Высокопоточная оксигенотерапия – это метод кислородной терапии, при использовании которого обеспечивается доставка подогретой и увлажненной кислородо-воздушной смеси через специальные носовые канюли при высоких скоростях потока (до 60 литров в минуту). При этом имеется возможность обеспечить FiO2 до 1,0.
Высокопоточная оксигенотерапия эффективна при тяжелой степени гипоксемической острой дыхательной недостаточности (ОДН) – с индексом PaO2 / FiO2 менее 150 мм рт. ст. (сатурация на воздухе без кислорода ниже 75%).
Одним из важных физиологических свойств высокого потока для COVID-пациентов является эффект промывания анатомического мертвого пространства. Это приводит к улучшению элиминации углекислого газа и уменьшению работы дыхания пациента, объема анатомического мертвого пространства, увеличению оксигенации и генерированию невысокого (1–4 мбар) положительного давления в гортано-глотке и трахее (СРАР – подобный эффект) — см. рис. 7.
Прон-позиция — лечение лежа на животе

Прон-позиция – один из способов сохранить легкие. Позиция тела «лежа на животе» используется для пациентов с коронавирусной инфекцией. Она
✅способствует равномерному распределению крови и жидкости в лёгких;
✅препятствует развитию и прогрессированию отёка и вирусной пневмонии;
✅включает слабо задействованную дыхательную мускулатуру;
✅приводит к снижению образования фиброза легких.
При этом необходимо подкладывать подушки под голову, грудь и таз.
Цель прон-позиции – увеличить объем вентилируемых легких за счет нижних и задних отделов. Лопатки раздвигаются и позволяют легким расправиться без повышенного давления в дыхательных путях.
Прон-позиция проводится не реже двух раз в сутки (оптимально общее время на животе 12-16 часов в сутки). Раннее применение прон-позиции в сочетании с кислородотерапией или с неинвазивной ИВЛ помогает избежать интубации у многих пациентов.
Основные механизмы действия прон-позиции
расправление гравитационно-зависимых ателектазов;
улучшение вентиляционно-перфузионных соотношений;
улучшение дренажа секрета дыхательных путей;
на фоне СРАР вентиляция распределяется более равномерно.
У пациентов с выраженным ожирением и у беременных на поздних сроках вместо прон-позиции предпочтительнее использовать положение лежа на боку со сменой стороны несколько раз в сутки.
Противопоказания к самостоятельной прон-позиции
нарушение сознания (угнетение или ажитация);
гипотензия;
недавняя операция на брюшной или грудной полостях;
выраженное ожирение;
массивное кровотечение;
повреждения спинного мозга;
нарушения ритма, могущие потребовать дефибрилляции и/или массажа сердца.
Особенность
Поражения легких при COVID-19 отличаются выраженной артериальной гипоксемией, часто не соответствующей объёму поражения и степени снижения податливости лёгочной ткани. Это связано с феноменом избыточной перфузии пораженных альвеол при COVID-19 (расширение сосудов) и несоответствием между вентиляцией и перфузией.
При развитии ОРДС у этих пациентов, как правило, нет других причин для интубации трахеи.
К последним (причинам для интубации) относятся:
нарушения сознания,
мышечная слабость (дисфункция диафрагмы при полинейромиопатии критических состояний);
нестабильная гемодинамика;
интраабдоминальная гипертензия;
низкая податливость грудной стенки;
нарушения биомеханики дыхания, ведущие к повышенной работе дыхания.
Вследствие этого у значимой части таких пациентов компенсация гипоксемии и острой дыхательной недостаточности достигается неинвазивными методами – оксигенотерапией и неинвазивной ИВЛ, даже при снижении индекса PaO2/FiO2 до 100 мм рт. ст., а у некоторых – и ниже.
У пациентов с COVID-19 формируются ателектазы в дорсальных отделах легких, в связи с чем самостоятельная прон-позиция (положение лежа на животе) высокоэффективна и у неинтубированных пациентов, которые получают кислородотерапию или неинвазивную ИВЛ.
Алгоритм «Аппаратная неинвазивная вентиляция легких»
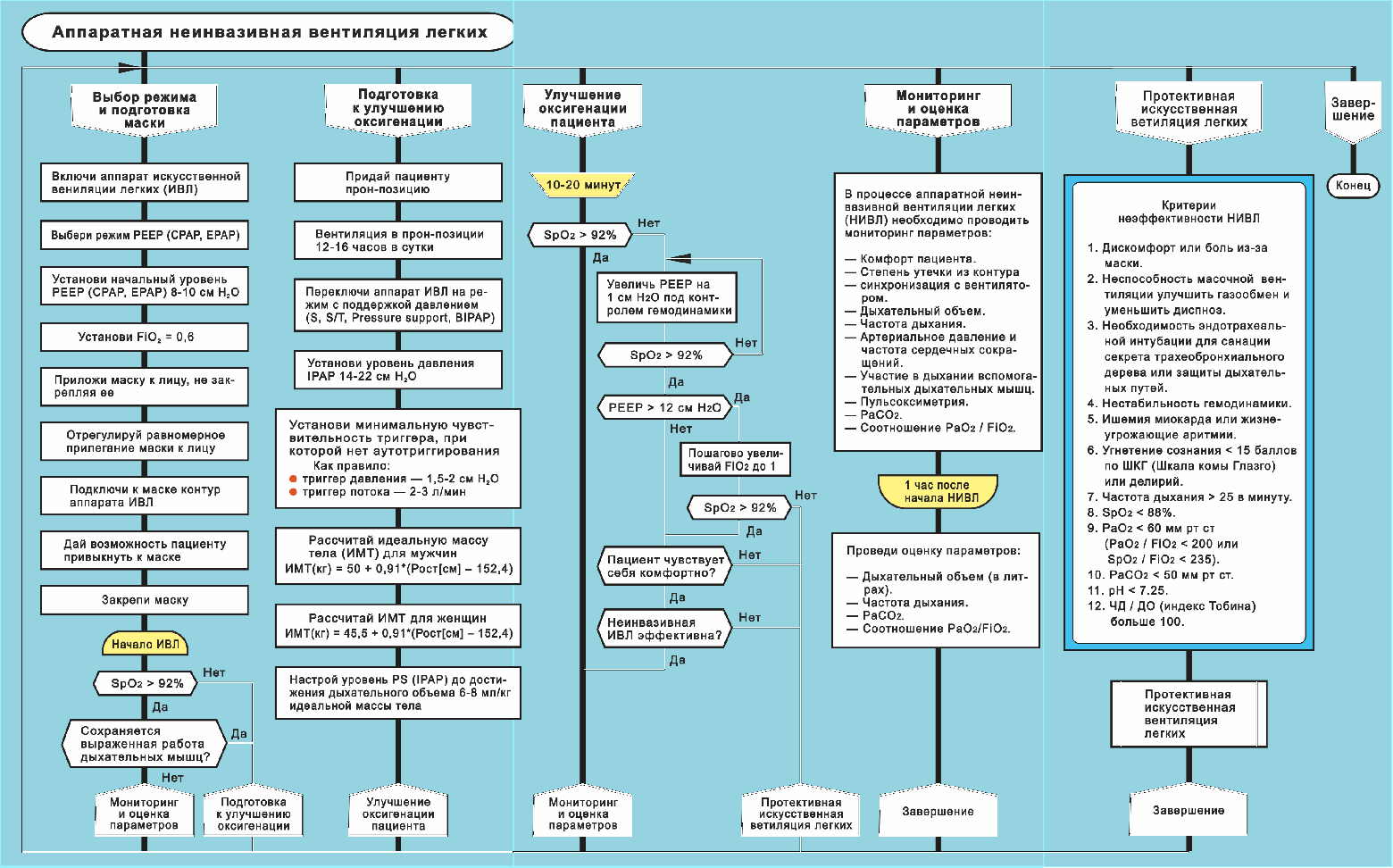
Рис. 8. Алгоритм «Аппаратная неинвазивная вентиляция легких».
Чтобы улучшить читаемость рисунка 8, ниже он представлен разбитым на три части.
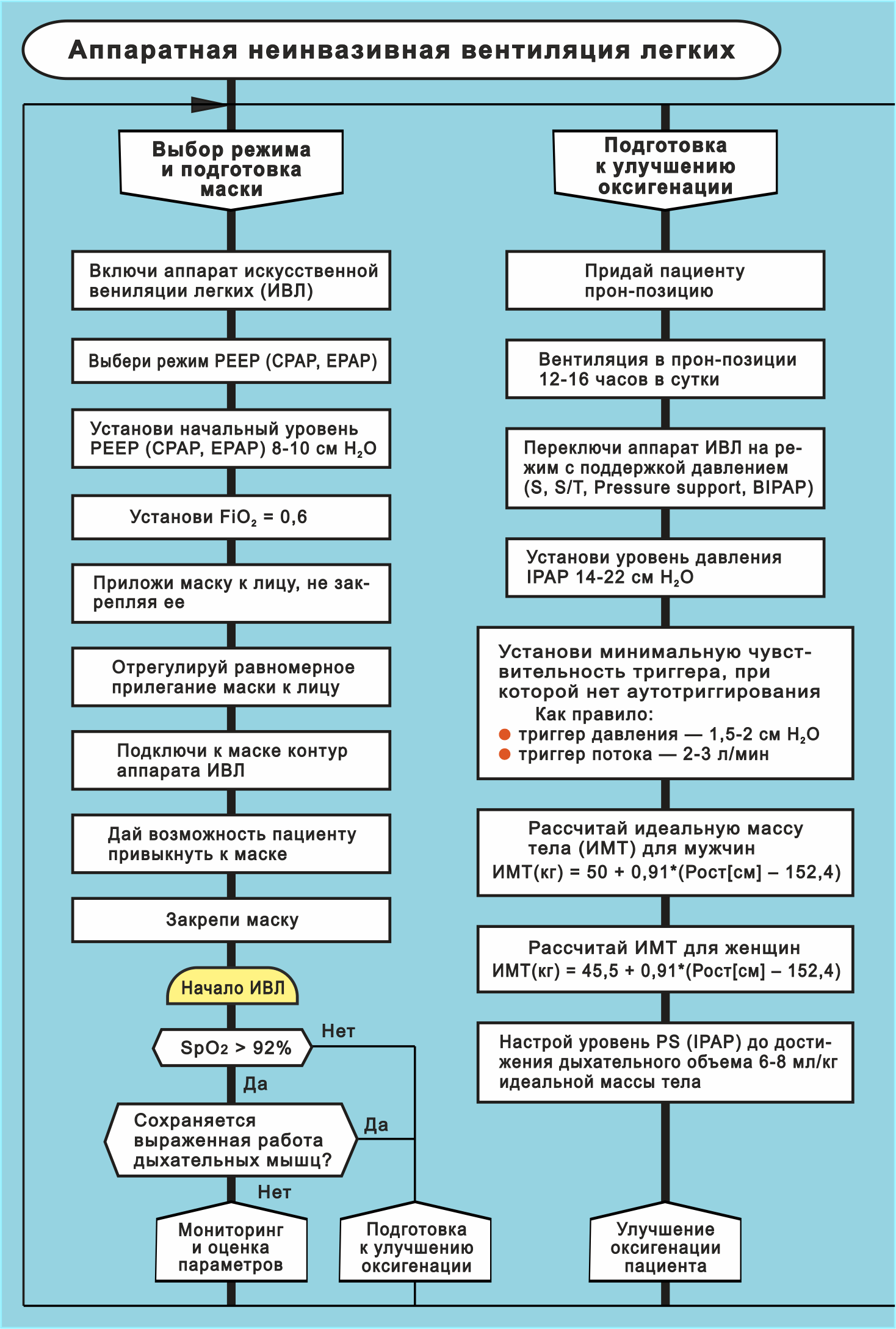
Рис. 8а. Алгоритм «Аппаратная неинвазивная вентиляция легких». Показаны две ветки силуэта:
1 «Выбор режима и подготовка маски» и
2 «Подготовка к улучшению оксигенации»
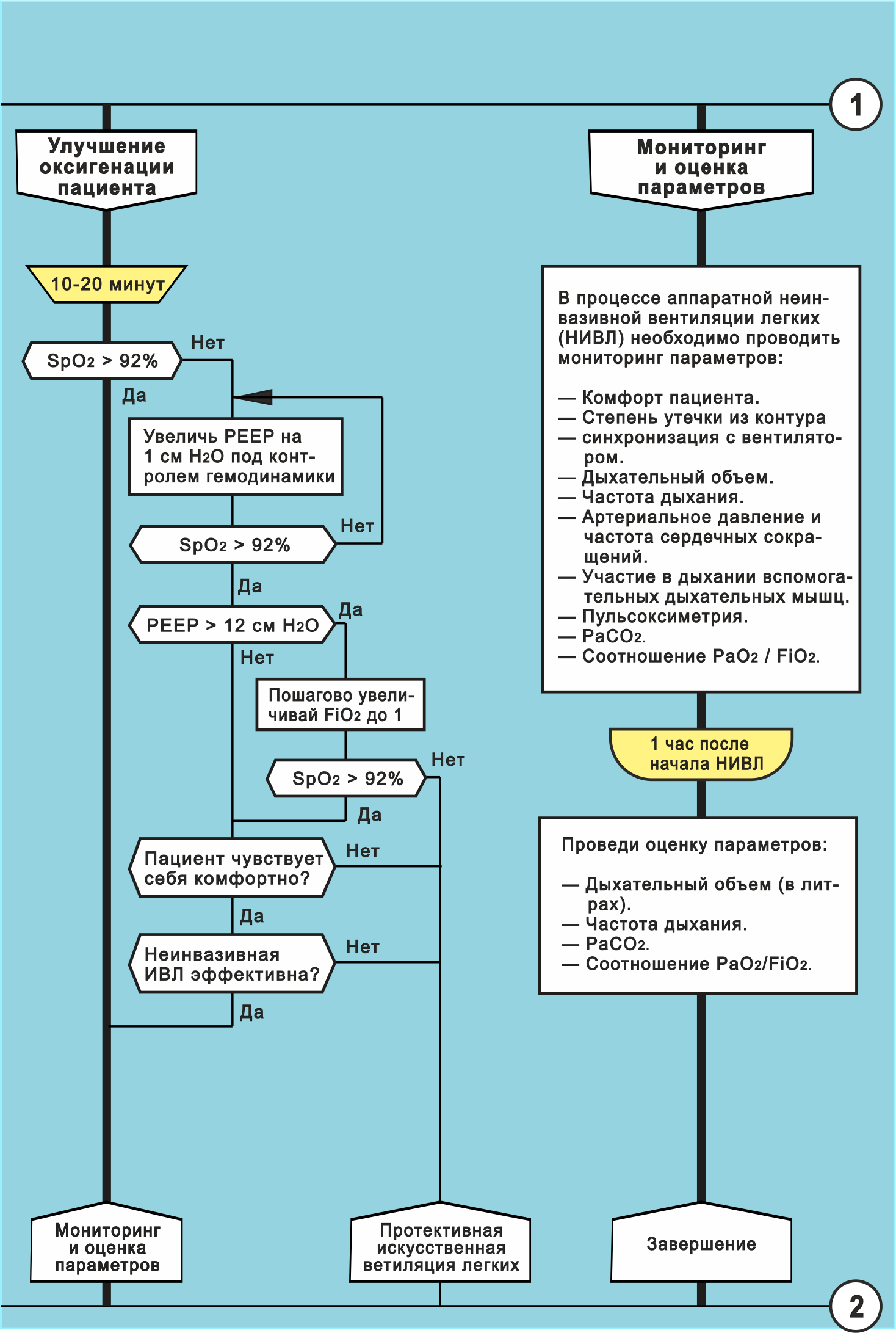
Рис. 8б. Алгоритм «Аппаратная неинвазивная вентиляция легких». Показаны две ветки силуэта:
3 «Улучшение оксигенации пациента» и
4 «Мониторинг и оценка параметров»

Рис. 8в. Алгоритм «Аппаратная неинвазивная вентиляция легких». Показаны две ветки силуэта:
5 «Протективная искусственная вентиляция легких» и
6 «Завершение»
В данном параграфе описан алгоритм НИВЛ — неинвазивной искусственной вентиляция легких (рис. 8).
При проведении НИВЛ рекомендовано использовать:
специализированные аппараты для НИВЛ;
универсальные аппараты ИВЛ в режиме НИВЛ, в которых компенсируются утечки;
специализированные лицевые маски, носовые маски или шлемы, так как это повышает эффективность и безопасность НИВЛ.
Следует отметить, что эффективность использования специализированных аппаратов НИВЛ выше.
Кроме того, существуют аппараты для домашней НИВЛ.
Ввиду невысокой рекрутабельности альвеол и отсутствии выраженной внелегочной патологии у большинства пациентов с COVID-19 неинвазивная ИВЛ становится одним из основных методов респираторной поддержки, вытесняя инвазивную ИВЛ.
Неинвазивная ИВЛ показана при неэффективности низкопоточной и высокопоточной оксигенотерапии.
Когда следует использовать неинвазивную ИВЛ
Применение НИВЛ рекомендовано только при следующих условиях:
Сохранность сознания, стабильная гемодинамика.
Возможность сотрудничать с персоналом.
Отсутствие клаустрофобии (при применении шлемов).
Сохранность механизма откашливания мокроты.
НИВЛ не рекомендуется, если имеет место
Отсутствие самостоятельного дыхания (апноэ).
Нестабильная гемодинамика (гипотензия, ишемия или инфаркт миокарда, жизнеугрожающая аритмия, неконтролируемая артериальная гипертензия).
Невозможность обеспечить защиту дыхательных путей (нарушение кашля и глотания) и высокий риск аспирации.
Избыточная бронхиальная секреция.
Признаки нарушения сознания (возбуждение или угнетение сознания), неспособность пациента к сотрудничеству.
Травма или ожог лица, анатомические дефекты, препятствующие установке маски.
Неспособность пациента убрать маску с лица в случае рвоты.
Активное кровотечение из желудочно-кишечного тракта.
Обструкция верхних дыхательных путей.
Дискомфорт от маски.
Маски и шлемы для неинвазивной ИВЛ
Для неинвазивной ИВЛ могут быть использованы специальные маски для НИВЛ (ороназальные и полнолицевые), а также шлемы (для СРАР и для НИВЛ, в зависимости от выбранного режима и типа контура аппарата).
При использовании ороназальных и полнолицевых масок НИВЛ следует обратить внимание на следующие моменты:
если применен стандартный аппарат ИВЛ с двухшланговым контуром и наличием клапана выдоха, то следует использовать невентилируемые маски (без утечки в «колене» маски);
если применен специализированной аппарат для НИВЛ с одношланговым контуром, то при наличии порта выдоха в контуре используют маски с невентилируемым «коленом». При отсутствии такого порта применяют маски с вентилируемым «коленом»;
оптимальная утечка составляет около 30 литров в минуту. При снижении утечки менее 7 литров в минуту следует ослабить маску. При утечке 30-60 литров в минуту надо плотно прикрепить маску. При утечке более 60 литров в минуту —сменить маску;
следует подбирать оптимальный размер маски в соответствии с размером лица пациента, большинству взрослых пациентов подойдут маски размера М;
при развитии пролежней от маски следует сменить маску на другой тип (ротация маски), например, ороназальную на полнолицевую. Для профилактики пролежней рекомендовано использовать ротацию масок и специальные гелевые адгезивные пластыри (протекторы).
При использовании шлемов для НИВЛ следует обращать внимание на соответствие между типом шлема, типом контура, выбранным режимом ИВЛ и типом аппарата ИВЛ.
Стартовый режим неинвазивной ИВЛ
Стартовым режимом НИВЛ является СРАР (ЕРАР) 8–10 см вод. ст. и инспираторная фракция кислорода 0,6 — см. рис. 8. При сохранении на этом фоне выраженной работы дыхательных мышц шеи следует переключить аппарат на режим с поддержкой давлением (S, S/T, Pressure Support, BIPAP) с уровнем давления IPAP 14–22 см вод. ст.
Далее нужно подобрать минимальное инспираторное давление, при котором сохраняется комфорт пациента и нет видимой работы дыхания пациента. Уровень FiO2 следует подбирать на основе целевого значения оксигенации.
При проведении НИВЛ следует следить за величиной выдыхаемого дыхательного объема, которая не должна превышать при ороназальной и полнолицевой маске 9 мл/кг идеальной массы тела. При шлеме может быть на 50-75% выше ввиду высокой податливости и большого объёма мёртвого пространства шлема.
Высокие уровни PEEP/CPAP (больше 12 см вод. ст.) и/или PS (больше 20 см вод. ст.), несмотря на временное улучшение оксигенации, приводят к дискомфорту больного и снижению эффективности НИВЛ (рис. 8).
Уменьшение диспноэ, как правило, достигается вскоре после настройки адекватного режима вентиляции, в то время как коррекция гиперкапнии и/или гипоксемии может требовать нескольких часов.
Последовательность действий
В первые часы вспомогательная неинвазивная вентиляция легких должна проводиться в постоянном режиме. Далее, после постепенного снижения респираторной поддержки, возможен переход на НИВЛ сеансами по 3-6 часов в день вплоть до полной ее отмены. При уменьшении степени поражения лёгких, снижения потребности в кислороде следует поэтапно снижать:
сначала FiO2,
затем уровень инспираторного давления (IPAP, Pressure Support),
затем уровень СРАР (ЕРАР).
При прогрессировании заболевания задержка интубации трахеи может приводить к ухудшению прогноза.
Критерии неэффективности НИВЛ
Дискомфорт или боль, вызванная маской.
Неспособность масочной вентиляции улучшить газообмен или уменьшить диспноэ.
Необходимость эндотрахеальной интубации для санации секрета трахеобронхиального дерева или защиты дыхательных путей.
Нестабильность гемодинамики.
Ишемия миокарда или жизнеугрожающие аритмии.
Угнетение сознания меньше 15 баллов по шкале комы Глазго или делирий.
Частота дыхания больше 25 раз в минуту.
Уровень насыщения крови кислородом SpO2 меньше 88%.
PaO2 < 60 мм. рт. ст. (PaO2/FiO2 < 200 или SpO2/FiO2 < 235).
PaCO2 > 50 мм. рт. ст.
Показатель кислотности pH < 7.25.
Индекс Тобина (Частота дыхания/Дыхательный объем) больше 100.
Алгоритм «Протективная искусственная вентиляция легких»

Рис. 9. Алгоритм «Протективная искусственная вентиляция легких»
Алгоритм описывает процесс перевода пациента на протективную ИВЛ и подбор параметров вентиляции (рис. 9).
Интубация трахеи — это установка эндотрахеальной трубки с целью обеспечения проходимости дыхательных путей и проведения искусственной вентиляции легких.
Укажем показания для интубации трахеи (достаточно одного критерия):
Гипоксемия (SpO2 меньше 92%), несмотря на высокопоточную оксигенотерапию или НИВЛ в положении лежа на животе с FiO2 100%.
Усталость пациента на фоне высокопоточной оксигенации или НИВЛ в прон-позиции с FiO2 = 1,0.
Нарастание видимых экскурсий грудной клетки и/или участие вспомогательных дыхательных мышц, несмотря на высокопоточную оксигенацию или НИВЛ в положении лежа на животе с FiO2 = 1,0.
Угнетение сознания или возбуждение.
Остановка дыхания.
Нестабильная гемодинамика (рис. 9).
Средства индивидуальной защиты медицинского персонала
При проведении интубации трахеи персоналу отделений анестезиологии, реанимации и интенсивной терапии рекомендуется использовать средства индивидуальной защиты 3-го уровня:
респираторы типа NIOSH-certified N95 или FFP3 классов защиты. В Европе стандарту N95 соответствует стандарт EN 149:2001+А1:2009 “Respiratory protective devices — Filtering half masks to protect against particles”. Можно использовать электроприводной воздухоочистительный респиратор с капюшоном (powered air-purifying respirator, PAPR);
двойные перчатки — один комплект синих нитриловых перчаток (внутренняя перчатка) соответствующего размера и один комплект хирургических перчаток с длинными манжетами (внешняя перчатка) соответствующего размера;
медицинская шапочка одноразовая;
водонепроницаемый халат с длинным рукавом + фартук, или защитный комбинезон с капюшоном, или противочумный костюм;
средства защиты глаз и кожи лица (полнолицевая защитная маска, защитный экран + защитные очки закрытого типа);
обувь, непроницаемая для жидкостей, с возможностью дезинфекции, бахилы.
Ассистенты при выполнении данных процедур должны надевать респираторы N95, FFP3 или аналогичные, шапочки, водонепроницаемый халат с длинным рукавом, средства защиты глаз и двойные перчатки.
Рекомендуется планировать интубацию трахеи заранее, поскольку необходимо время для сбора команды и надевания средств индивидуальной защиты.
Необходимо минимизировать число участников процедуры интубации трахеи. Все потенциально необходимые специалисты, не участвующие в интубации с самого ее начала, должны находиться в готовности в другом помещении с надетыми средствами индивидуальной защиты.
Выполнять интубацию трахеи пациентам с COVID-19 рекомендуется анестезиологу-реаниматологу, обладающему наибольшим опытом работы, чтобы свести к минимуму количество попыток и риск передачи инфекции.
Особенности алгоритма
У пациентов с прогрессирующими нарушениями газообмена, которым уже проводится высокопоточная оксигенация через назальные канюли, неинвазивная вентиляция, рекомендуется их применение как самостоятельного метода преоксигенации или в комбинации с другими методами оксигенации во время подготовки к интубации.
У пациентов с новой коронавирусной инфекцией (НКИ) без прогрессирующих нарушений газообмена, которым выполнение интубации и перевод на ИВЛ показаны в связи с иными причинами (нарушения сознания, риск обструкции ВДП и т. д.), рекомендуется проводить предварительную оксигенацию по стандартной методике 100% кислородом с потоком не более 10 литров в минуту в положении с приподнятым головным концом кровати на 45 градусов, с использованием тщательно подобранной и герметично прижатой лицевой маски, соединенной с респиратором.
Рекомендуется проводить преоксигенацию не менее 5 минут или до достижения максимально возможного уровня EtO2 (оптимально выше 90 %) и SpO2.
У всех пациентов с COVID-19 или подозрением на COVID-19 при отсутствии прогнозируемых «трудных дыхательных путей» рекомендуется применять методику быстрой последовательной индукции (rapid sequence induction).
Быстрая последовательная индукция
Выбор гипнотика следует осуществлять с учетом состояния пациента (кетамин, пропофол, бензодиазепины), дозы миорелаксантов составляют 1,5–2 мг/кг для сукцинилхолина или 1,2 мг/кг для рокурониума. Рокурониум является препаратом выбора вследствие низкого риска развития кашля и образования аэрозоля.
Необходимо строго контролировать время от введения миорелаксантов до развития тотальной миоплегии (при наличии — с помощью нервно-мышечного мониторинга). Это нужно для минимизации развития кашля на фоне преждевременных попыток ларингоскопии или десатурации на фоне необоснованно затянувшейся паузы апноэ.
При нестабильной гемодинамике рекомендуется обеспечить вазопрессорную поддержку до начала индукции. При наличии высокого риска аспирации следует применять прием Селлика, учитывая риск развития кашля в ответ на преждевременное увеличение давления на перстневидный хрящ.
После выключения сознания следует проводить апнейстическую оксигенацию через плотно прижатую лицевую маску с потоком не выше 6 литров в минуту либо продолжать применение методов, использованных для преоксигенации.
Проведение ИВЛ во время индукции следует минимизировать, использовать лишь при риске развития десатурации (SpO2 < 92 %). Следует применять VE-метод прижатия лицевой маски, использовать сниженное давление в дыхательных путях, своевременно применять орофарингеальные воздуховоды.
Инвазивная искусственная вентиляция легких
Инвазивная ИВЛ при терапии COVID-ассоциированной острой дыхательной недостаточности применяется в случае неэффективности неинвазивной ИВЛ или недоступности последней.
ИВЛ направлена не только на обеспечение адекватного газообмена, стабилизацию коллабированных альвеол, но и на минимизацию потенциального индуцированного пациентом или ятрогенного повреждения легких.
При применении инвазивной ИВЛ при неэффективности неинвазивной ИВЛ следует иметь в ввиду, что в большинстве случаев применение вспомогательных режимов ИВЛ на фоне ясного сознания или умеренной седации после интубации трахеи может усиливать повреждение лёгких.
Поэтому в первые несколько часов после интубации трахеи следует использовать полностью управляемые режимы ИВЛ на фоне глубокой седации и/или миоплегии (рис. 9).
Искусственная вентиляция легких у пациентов с COVID-19
При ИВЛ у пациентов с COVID-19 рекомендован дыхательный объем 6 мл/кг идеальной массы тела. Применение дыхательного объёма более 6 мл/кг ИМТ ведет к росту осложнений и летальности.
Для предупреждения повреждения легких во время проведения ИВЛ необходимо предотвращать избыточное повышение давления в альвеолах (баротравму легких), поступление избыточного объема воздуха в легких (волюмотравму) и повторение циклов закрытия–раскрытия альвеол (ателектотравму).
Указанные принципы составляют основу лечебной доктрины, называемой «открытыми отдыхающими легкими» («open lung rest»). В многочисленных экспериментальных и клинических работах показано, что невнимание к этим факторам приводит к прогрессированию дисфункции легких и развитию не только дыхательной, но и полиорганной недостаточности из-за выброса из альвеолоцитов повреждающих медиаторов воспаления.
Цепь описываемых событий имеет название биотравмы. Для предупреждения баротравмы альвеолярное давление должно быть ограничено величиной 30 см вод. ст. Если у пациента нет проблем с податливостью грудной клетки, то величина давления плато в дыхательных путях соответствует альвеолярному давлению.
Поэтому при проведении ИВЛ стараются не превышать давление плато более чем 30 см вод. ст. Для ограничения давления плато при снижении податливости легких приходится уменьшать вводимый дыхательный объем (рис. 9).
Безопасная искусственная вентиляция легких
Проведение «безопасной» ИВЛ возможно в режимах как с управляемым давлением (PC), так и с управляемым объемом (VC). При этом желательно использовать нисходящую форму инспираторного потока, обеспечивающую лучшее распределение газа в легких и меньшее давление в дыхательных путях.
Мы начинаем ИВЛ с режима управления по объему, так как на данном режиме проще подобрать PEEP в рамках протективной вентиляции. После подбора РЕЕР можно перейти в любой комфортный для пациента режим с учетом дыхательного объема в пределах 4–8 мл/кг идеальной массы тела.
У пациентов с PaO2/FiO2 выше 150 мм рт. ст. при реверсии миоплегии рекомендовано, при технической возможности и отсутствии патологических ритмов дыхания, перейти на полностью вспомогательный режим вентиляции (в большинстве аппаратов – PSV) для улучшения распределения газа, профилактики ателектазирования и атрофии диафрагмы.
У пациентов с COVID-19 при проведении ИВЛ рекомендовано использовать РЕЕР в зависимости от рекрутабельности альвеол и риска образования ателектазов. У пациентов с COVID-19 отмечена невысокая рекрутабельность альвеол, стартовая величина эффективного и безопасного РЕЕР составляет 8–10 см вод. ст.
Пациенты с острым респираторным дистресс-синдромом
У пациентов с ОРДС и внутрибрюшной гипертензией (давление в мочевом пузыре более 15 мм рт. ст.) рекомендовано установить РЕЕР не ниже 10 мбар для предотвращения ателектазирования лёгких.
У пациентов с ОРДС и индексом массы тела выше 30 кг/м2 рекомендовано установить РЕЕР не ниже 10–12 мбар, а при сочетании высокой рекрутабельности и индекса массы тела выше 40 кг/м2 величина РЕЕР может составлять до 24 мбар, так как это приводит к уменьшению ателектазирования лёгких, улучшению оксигенации и вероятному снижению летальности.
У пациентов с ОРДС вследствие COVID-19 при проведении ИВЛ рекомендовано использовать неинвертированное соотношение вдоха к выдоху для более равномерного распределения газа в легких и снижения отрицательного влияния ИВЛ на постнагрузку правого желудочка.
Рутинное применение инверсного соотношения вдоха к выдоху (более 1 к 1,2) не рекомендовано, при этом необходимо избегать неполного выдоха (экспираторный поток перед началом вдоха аппарата должен достигать нуля). Следует регулировать частоту дыхания для достижения нормокапнии, но не более 30 раз в минуту. Для вдоха достаточно времени 0,8–1,2 секунд (рис. 9).
Пациенты с COVID-19
При ИВЛ у пациентов с COVID-19 рекомендовано положение лежа на животе в течение не менее 16 ч в сутки для улучшения оксигенации и возможного снижения летальности.
Пациента следует положить на живот, предварительно подложив валики под грудную клетку и таз, а также подушку для лица (желательно использовать специальные подушки для прон-позиции) с таким расчетом, чтобы живот не оказывал избыточного давления на диафрагму, а также не создавались условия для развития пролежней лица (рис. 9).
При выраженном ожирении вместо прон-позиции при проведении ИВЛ предпочтительно положение лежа на боку со сменой стороны несколько раз в сутки.
Осложнения
Осложнения при вентиляции в положении лежа на животе таковы:
Перегибы и дислокации интубационных трубок и венозных катетеров.
Трудность выполнения сердечно-легочной реанимации.
Развитие невритов периферических нервов верхних конечностей.
Повреждение носа и глаз – лицевой и периорбитальный отек – развивается почти в 100% случаев; кератоконьюктивит, требующий лечения, развивается у 20% пациентов.
В прон-позиции затруднены санация полости рта и трахеи, обработка глаз, лица.
Критерий прекращения прон-позиции: увеличение PaO2/FiO2 больше 200 мм рт.ст. при PEEP меньше 10 см вод. ст., сохраняющееся больше 4 часов после последнего сеанса прон-позиции.
Конец медицинской части статьи и обсуждение
На этом можно закончить профессиональную медицинскую часть. Цель статьи — познакомить читателей с примерами клинических алгоритмов на актуальную тему: лечение коронавирусной инфекции COVID-19. Цель выполнена.
Мы рассмотрели четыре алгоритма:
Низкочастотная оксигенация пациента.
Неинвазивная высокопоточная оксигенация пациента.
Аппаратная неинвазивная вентиляция легких.
Протективная искусственная вентиляция легких.
Для каждого алгоритма показаны:
эргономичный (user-friendly) графический чертеж алгоритма высокой точности, представленный на медицинском языке ДРАКОН;
текстовое описание алгоритма, содержащее ссылки на чертеж дракон-схемы.
Сравнение медицинского языка ДРАКОН с графическими аналогами
Ближайших аналогов два:
Международный стандарт ISO 5807-85 и его калька межгосударственный стандарт ГОСТ 19.701-90.
Поведенческие диаграммы языка UML, прежде всего, диаграмма деятельности (activity diagram).
По сравнению с ГОСТ 19.701-90 язык ДРАКОН имеет значимые преимущества — см. здесь.
По сравнению с UML предполагается наличие преимуществ, однако подтверждающих документов мало — см. drakon vs uml.
Попутное замечание
Хабр — сообщество разработчиков. Возникает вопрос: должны ли в это сообщество входить разработчики клинических алгоритмов, то есть профессиональные врачи?
Это откроет для Хабра новые перспективы. ИТ-сообщество Хабра сможет напрямую контактировать (обмениваться знаниями) с медицинским сообществом и содействовать цифровой трансформации медицины, включая слабо развитые, но актуальные области, такие как клинические алгоритмы.
Первые шаги в этом направлении сделаны. Медицина на Хабре де факто уже есть. Вот пример — Артем Газаров, основатель сети клиник Белая радуга (стоматология). На Хабре 27 публикаций, карма 131.
Другой пример — Татьяна Шилова, профессор, доктор медицинских наук, главврач «Клиники профессиональной офтальмологии доктора Шиловой». Татьяна Шилова успела опубликовать на Хабре 52 статьи и полтыщи комментариев, причем все — по медицине. И заработала карму 134.
Что отсюда следует? Мне кажется, медицину на Хабре желательно узаконить и создать два новых хаба: «Медицина» и «Клинический алгоритм».
